Lezing - onderzoek naar oorzaak van artrose
Beknopt verslag van de lezing van Dr. Ingrid Meulenbelt van het Leiden Universitair Medisch Centrum over het artrose onderzoek bij de afdeling Moleculaire Epidemiologie. In 2000 is zij begonnen met het onderzoeken van artrose via het DNA.
Per jaar krijgen 650.000 mensen deze diagnose artrose, waaronder 25.000 jonge patiënten tussen de 25 en de 44 jaar. Er is dan op de röntgenfoto’s sprake van versmalling van de gewrichtsspleet door verlies van kraakbeen, veranderingen in het onderliggend bot en vorming van osteofyten. Een probleem bij het onderzoek is dat er een onduidelijke relatie is tussen de radiologische kenmerken van artrose op de foto’s en de pijn en klachten die de patiënt zelf ervaart.
Ingrid somt de symptomen op van artrose, daarbij al aangevend dat die bij de aanwezigen wel bekend zullen zijn:
• Stijfheid
• Pijn
• Crepiteren (kraken van de gewrichten)
• Bewegingsbeperking
• Invaliditeit
De risicofactoren voor het krijgen van artrose zijn:
• Leeftijd
• Overgewicht
• Geslacht (vrouwen hebben vaker artrose dan mannen)
• Bot dichtheid
• Erfelijkheid
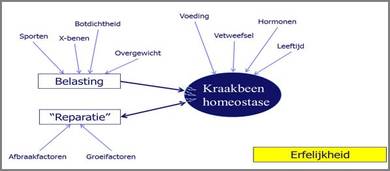
Ingrid legt uit dat mensen met overgewicht ook vaker hand artrose krijgen. De relatie tussen overgewicht en artrose loopt dus zeer waarschijnlijk niet alleen via overbelasting. De ontstekingsfactoren die uitgescheiden worden door vetcellen hebben waarschijnlijk een negatief effect op de gezondheid van het kraakbeen. Het exacte mechanisme is echter nog niet helemaal duidelijk. Schade aan het bot of kraakbeen door trauma’s zoals bij een val of een ongeluk, kan er uiteraard ook toe bijdragen dat in het gewricht artrose ontstaat.
Er is op dit moment geen behandeling / medicijn die het artrose proces daadwerkelijk vertraagt of geneest. Behandeling van artrose bestaat daarom momenteel uit:
• Bewegingstherapie
• Ontstekingsremmers
• Gewrichtsvervanging
Op een vraag uit de zaal of sporten dan niet goed is voor mensen met artrose, antwoordt Ingrid dat beweging goed is voor gewrichten maar dat overbelasting of piekbelasting van de (aangetaste) gewrichten moet worden vermeden.
Het uittesten van nieuwe medicijnen is zeer kostbaar omdat:
• Het verlies van kraakbeen en de botveranderingen langzaam voortschrijdt. Het uittesten van medicijnen moet dus plaatsvinden over een lange periode om veranderingen te kunnen waarnemen.
• Kleine veranderingen in het kraakbeen en bot moeilijk zijn waar te nemen op röntgenfoto’s.
• Een röntgenfoto niet laat zien of het ziekteproces actief is of in remissie.
Het onderzoek bij de afdeling Moleculaire Epidemiologie richt zich ook op het vinden van nieuwe gevoelige ‘markers’ van het artrose proces in bloed of urine. Er wordt dan gekeken naar bijvoorbeeld afbraakproducten van kraakbeen en bot of ontstekingsparameters.
Artrose is een zeer complexe ziekte:
• Heterogeniteit in ziektebeeld (heup, knie hand).
• Heterogeniteit in gevoeligheid van artrose (overgewicht, erfelijkheid, belasting).
• Weinig inzicht in de onderliggende zaken en zeer waarschijnlijk zijn dit er vele.
• Er zijn geen gevoelige metingen die veranderingen of activiteit van het ziekteproces in het kraakbeen weergeven.
• De erfelijkheid m.b.t. artrose is erg complex en wordt waarschijnlijk veroorzaakt door vele verschillende erfelijke eigenschappen (genen).
Onderzoekers hebben in een- en twee-eiige tweelingen met artrose vastgesteld hoe erfelijk artrose is. Doordat eeneiige tweelingen (genetisch identiek) vaker samen artrose hebben in vergelijking tot twee-eiige tweelingen (voor 50% genetisch identiek) is vastgesteld dat artrose erfelijk is. Het onderzoek van de groep van Ingrid is erop gericht om vast te stellen welke eigenschappen deze erfelijkheid bepalen. Een vergelijking; de kleur van je ogen is erfelijk want eeneiige tweelingen hebben altijd dezelfde kleur ogen en twee-eiige tweelingen “maar” in 50% van de gevallen. De erfelijke eigenschap “pigment” bepaald de kleur van ogen.
Bij het zoeken naar de erfelijke eigenschappen (genen) die het ontstaan van artrose veroorzaken wordt gebruik gemaakt van variaties in de lettercode het DNA. Het DNA heeft 4 “letters” C, G, A, T, die de woorden (eigenschappen) van een individu beschrijven. Aangezien de eigenschappen tussen personen net even anders zijn door variaties in de lettercodes kunnen we onderzoekers van elkaar onderscheiden. Ontdekken van de genen die de erfelijke aanleg beïnvloeden kan inzicht geven in het mechanisme die het ontstaan van artrose beïnvloeden.
Waarom gaat iemand sneller achteruit dan de ander?
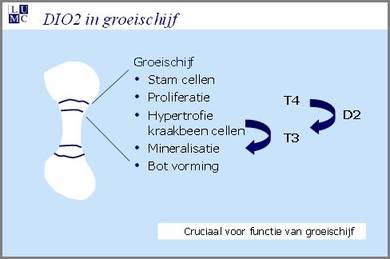
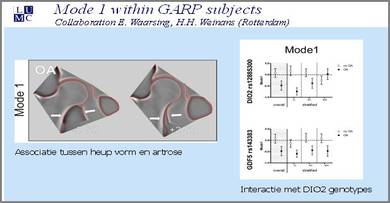
In 2008 hebben de onderzoekers van de groep van Ingrid ontdekt dat variaties in het DIO2 gen gerelateerd zijn aan artrose. Dit DIO2 gen activeert het schildklierhormoon in specifieke weefsels en cellen waaronder de groeischijf. Tijdens de ontwikkeling en bij de lengte groei van botten bij kinderen tot 18 jaar speelt de groeischijf een belangrijke rol. De groeischijf bestaat uit een schijf van kraakbeen in het bot waar kraakbeen cellen zich vermenigvuldigen om lengtegroei te bewerkstelligen. Activatie van het schildklierhormoon in de groeischijf op een specifiek moment op een specifieke plek zorgt ervoor dat het kraakbeen wordt afgebroken om plaats te maken voor bot. Verschillende artrose onderzoeksgroepen hebben eigenschappen (genen) ontdekt die de gevoeligheid voor artrose verhogen. Opmerkelijk is dat een belangrijk deel van deze eigenschappen betrokken zijn bij het regelen van het groeiproces in de groeischijf. Dit heeft ertoe geleid dat we nu aannemen dat een van de oorzaken van artrose ontstaat door afwijkingen in de vorm en opbouw van het skelet. Deze afwijkingen in de vorm van bijvoorbeeld het heup bot kan zorgen voor een overbelasting van het kraakbeen bij normaal gebruik van het gewricht.
Ingrid vertelt vervolgens dat de onderzoekers materiaal ter beschikking hebben om de afwijkingen in de activiteit van het gen te controleren in het kraakbeen. Ze verzamelen namelijk articulair kraakbeen van mensen met artrose die een prothese krijgen. Zo hebben zij kunnen constateren dat dragers een hogere activiteit van het artrose gen vertonen in het kraakbeen. Het artrose gen zorgt voor activatie van het schildklierhormoon en het schildklierhormoon zet het kraakbeen aan om af te breken om plaats te maken voor bot. Deze verhoogde activiteit van het artrose gen kan dus ook direct schadelijk zijn voor de gezondheid van het kraakbeen.
Het schadelijke effect van verhoogde activiteit van het artrose gen op de gezondheid van kraakbeen heeft Ingrid en haar onderzoeksgroep direct aangetoond in een kraakbeencel model in het laboratorium. In het laboratorium hebben zij laten zien dat wanneer je de activiteit van het artrose gen wordt verhoogd in kraakbeencellen, deze geen kraakbeenmatrix meer kunnen vormen. Remming van het artrose gen DIO2 daarentegen geeft een goede vorming van kraakbeen. De onderzoekers hebben dus in het laboratorium met behulp van het kraakbeen van artrose patiënten die een gewrichtsvervangende operatie ondergaan, de schadelijke effecten van het artrose gen kunnen vaststellen.
Op een vraag uit de zaal of er dan geen onderzoek kan plaats vinden door kraakbeen van de patiënten af te nemen antwoordt Ingrid dat dit zeker niet is aan te raden. Elke beschadiging / verstoring van het kraakbeen moet door het de kraakbeencel worden gerepareerd. Dit verhoogd het risico op vorming van “littekens” van het kraakbeen met daarmee een risico op vermindering van kwaliteit van het kraakbeen en een verhoging van het artrose risico.
De pijn bij artrose komt niet van het kraakbeen zelf want in het kraakbeen zitten geen zenuwen of bloedvaatjes, maar van de omliggende weefsels en van het bot.
De ene persoon ervaart meer pijn dan de ander. Waar dat aan ligt is niet duidelijk.
Conclusie bij een aantal leden: dus afvallen is tot nu toe de beste medicijn! Ingrid beaamt dat.